要点
- C12A7エレクトライドは電子濃度によって絶縁体から金属へと変化
- 絶縁体から金属へ変化するとアンモニア合成の触媒機能も劇的にジャンプ
- 高性能アンモニア合成触媒開発のための新たな道筋を提示
概要
東京工業大学応用セラミックス研究所の細野秀雄教授(元素戦略研究センターセンター長)と原亨和教授、北野政明准教授らは、常圧下で優れたアンモニア合成活性を持つ「ルテニウム担持12CaO・7Al2O3(C12A7)エレクトライド」[用語1]の電子濃度を高め、絶縁体から金属へと変化させると、反応メカニズムが劇的に変化し、従来の10倍以上の高い触媒活性が発現、また活性化エネルギー[用語2]が半分に低減することを発見した。電子濃度の異なるC12A7エレクトライド触媒を作成し、触媒特性を詳細に調べることにより実現した。
アンモニアは窒素肥料原料として膨大な量が生産されており、最近では水素エネルギーキャリアとしても期待が高まっている。穏和な条件でも作動する新触媒の開発により、アンモニア合成プロセスの省エネルギー化に向けた有力な手がかりが得られたといえる。従来、触媒活性は活性サイトという局所の性質で規定されるというのが一般的だったが、今回の結果はより広い範囲の電子状態が触媒活性をコントロールしていることを示している。半導体の電子物性の重要な現象が触媒機能と結びついたといえる。
アンモニア合成触媒はアルカリ金属化合物など様々な促進剤[用語3]が検討されてきたが、電子濃度を高めることで働く材料は見いだされていなかった。
研究成果は米国科学誌「ジャーナル・オブ・ザ・アメリカン・ケミカル・ソサイエティ(Journal of the American Chemical Society)」オンライン速報版に10月24日付で公開された。
研究の背景と経緯
人工的にアンモニアを合成する技術は、ハーバーとボッシュによって初めて見いだされ、この技術(ハーバー・ボッシュ法、HB法)は工業的に完成してから約100年経った現在でも、人類の生活を支えるために必要不可欠となっている。また、アンモニア分子は分解することで多量の水素発生源となり、かつ室温・10気圧で液体になることから、燃料電池などのエネルギー源である水素運搬の物質としても期待されている。
アンモニア合成を効率よく進めるために、鉄やルテニウムなどの触媒に、アルカリ金属やアルカリ土類金属の酸化物が添加されていた。しかし、これらの促進効果は不十分であり、安定な窒素分子の三重結合を効率よく切断することができず、その結果として、どの触媒を用いても窒素分子の結合を切断する過程が全体の反応の速度を遅くしていること(律速)が知られていた。
今回の研究に用いた触媒は細野教授らが2003年に開発したC12A7エレクトライドという物質の表面に、ナノサイズのルテニウムの微粒子を担持させたものであり、電子濃度によって、C12A7は絶縁体から金属へと転移することが知られていた。
研究成果
東工大の細野教授らは、電子濃度の異なるC12A7エレクトライド触媒を用いてアンモニア合成活性を詳細に調べたところ、C12A7エレクトライドが絶縁体から金属に変化する際に、触媒活性および反応メカニズムが劇的に変化する(スイッチする)ことを見いだした。
具体的には、C12A7エレクトライドの電子濃度が1.0× 1021 cm-3(立方メートル当たり)以下の場合は、触媒活性、活性化エネルギーともに既存の触媒とほぼ同じであるが、電子濃度が1.0× 1021 cm-3以上になると、触媒活性は電子濃度が低い場合よりも10倍程度高い値を示し、活性化エネルギーは約半分にまで低下することが分かった(図1)。
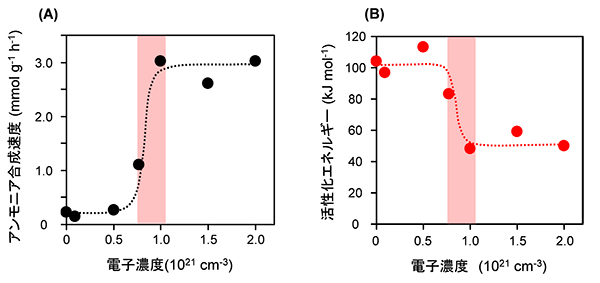
- 図1.
- さまざまな電子濃度のC12A7エレクトライドにルテニウムを担持した触媒を用いたアンモニア合成反応(A:アンモニア合成速度、B:活性化エネルギー)
電子濃度が1.0× 1021 cm-3を境に、反応速度との活性化エネルギーが大きく変化することが確認できる。
またルテニウム触媒を用いたアンモニア合成では反応速度は、水素の圧力が増加するにつれて低下する(水素の反応次数[用語4]が0または負の値となる)ことがよく知られている。これはルテニウムと水素の親和性が強く、ルテニウム表面が吸着した水素で覆われることにより、窒素の吸着が阻害される(水素被毒される)ためである。
C12A7エレクトライド触媒では、電子濃度が低い場合は、水素被毒されるが、電子濃度が1.0× 1021 cm-3以上になると、水素被毒されない(水素の反応次数が正の値となる)ことが分かった(図2)。つまり、水素圧力の増加に伴い、触媒活性が向上した。
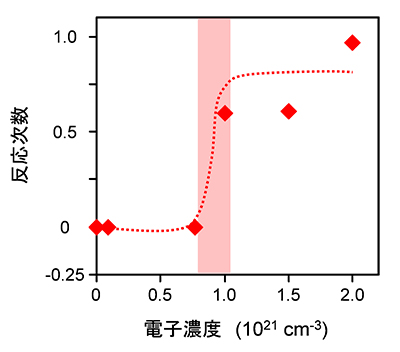
- 図2.
- さまざまな電子濃度のC12A7エレクトライドにルテニウムを担持した触媒の水素の反応次数
電子濃度が1.0× 1021 cm-3を境に、水素に対する反応次数が0から正の値へ変化することを確認できる。つまり電子濃度が高くなると水素被毒を受けなくなることが分かる。
以上の結果から電子濃度による反応メカニズムの違いをまとめると(図3)、電子濃度が1.0× 1021 cm-3以下の場合は、電気伝導性が悪く窒素分子の解離が効率よく起こらないため、既存の触媒と同様に、窒素分子の切断が律速段階[用語5]となる。さらに水素原子が触媒表面を覆う水素被毒の現象が起こる。
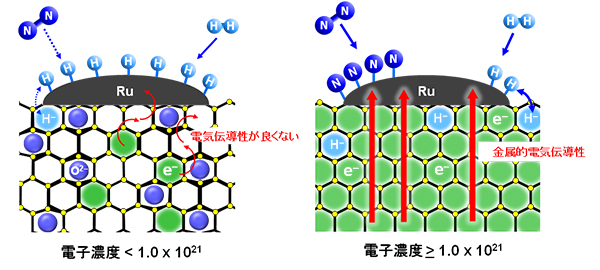
- 図3.
- 電子濃度の異なるC12A7エレクトライド上でのアンモニア合成のメカニズム
電子濃度が低いC12A7エレクトライド触媒では、電気伝導性が悪く、窒素の解離が効率よく起こらず、ルテニウム表面が水素で覆われる水素被毒が起こる。一方、電子濃度が高いC12A7エレクトライド触媒では、金属的電気伝導性を示し、窒素三重結合(N≡N)の切断が容易となり、ルテニウム上で切断された水素はケージ内にH-イオンとして取り込まれ、原子状水素として放出され窒素原子と反応しアンモニアが生じる。
一方、電子濃度が1.0× 1021 cm-3以上になると、金属的な電気伝導性を示すため、窒素分子の解離が効率よく起こり、窒素分子の切断が律速段階ではなくなる。また、ルテニウム上で切断された水素がC12A7エレクトライドのカゴの中にH-イオンとして収納されることで、ルテニウム上での水素被毒を防ぎ、このH-イオンが原子状水素として放出され、窒素原子と反応することでアンモニアが生成されると考えられる。このように電子濃度の違いにより反応メカニズムが大きく変化することを明らかにした。
今後の展開
今回の成果により、穏和な条件下で作動するアンモニア合成触媒では、電子注入効果と水素吸蔵効果が重要な役割を果たしていることが明確になった。従って、アンモニア合成プロセスの省エネルギー化に向けた触媒開発の有力な手がかりが得られたことになる。
研究の枠組み
本成果は、以下の事業・研究課題によって得られた。
戦略的創造研究推進事業 ACCEL
研究課題名 : |
「エレクトライドの物質科学と応用展開」 |
代表研究者 : |
東京工業大学 元素戦略研究センター長 細野秀雄 |
PM : |
科学技術振興機構 横山壽治
|
研究実施場所 : |
東京工業大学 |
研究開発期間 : |
平成25年10月~平成30年3月 |
用語説明
[用語1] C12A7エレクトライド : C12A7は12CaO・7Al2O3(酸化カルシウムと酸化アルミニウム化合物)でセメントの材料。
エレクトライドは電子がアニオンとして働く化合物の総称。通常の物質とは異なるユニークな性質を持つのではと関心を集めていたが、あまりに不安定なため、物性がほとんど不明のままだった。細野グループは、2003年に直径0.5ナノメートル程度のカゴ状の骨格が立体的につながった結晶構造をしているアルミナセメントに構成成分の1つC12A7を使って、安定なエレクトライドを初めて実現した。
このエレクトライドは金属のようによく電気を通し、低温では超伝導を示す。またアルカリ金属と同じくらい電子を他に与える能力を持つにもかかわらず、化学的にも熱的にも安定というユニークな物性を持っている。
[用語2] 活性化エネルギー : 反応の出発物質の基底状態から遷移状態に励起するのに必要なエネルギーのことであり、このエネルギーが小さいほど、その反応は容易になる。反応中に触媒が存在することで、活性化エネルギーを下げることが可能となる。
[用語3] 促進剤 : アンモニア合成において、活性な金属種であるルテニウムや鉄の近くに固定化され、それらの金属種に電子を与えることで、触媒表面上での窒素の解離反応を促進する物質。
[用語4] 反応次数 : アンモニア合成の反応速度(r)は、r = k(PN2)α(PH2)β(PNH3)γで表され、それぞれの反応ガス(N2,H2,NH3)の分圧に比例する。この式の指数部分(α,β,γ)が反応次数である。
[用語5] 律速段階 : 化学反応において最も遅い反応段階であり、この反応速度が全体の化学反応の速度を支配している。
論文情報
掲載誌 : |
Journal of the American Chemical Society |
論文タイトル : |
"Mechanism Switching of Ammonia Synthesis Over Ru-Loaded Electride Catalyst at Metal–Insulator Transition" (金属-絶縁体転移点におけるRu担持エレクトライド触媒上でのアンモニア合成メカニズムの変化) |
著者 : |
Shinji Kanbara,Masaaki Kitano,Yasunori Inoue, Toshiharu Yokoyam, Michikazu Hara, Hideo Hosono
|
DOI : |
問い合わせ先
(C12A7エレクトライドについて)
元素戦略センター センター長/応用セラミックス研究所
教授 細野秀雄
Email : hosono@msl.titech.ac.jp
Tel : 045-924-5009 / Fax : 045-924-5196
(触媒反応について)
応用セラミックス研究所
教授 原亨和
Email : mhara@msl.titech.ac.jp
Tel : 045-924-5311 / Fax:045-924-5381
(取材申し込み先)
東京工業大学 広報センター
Email : media@jim.titech.ac.jp
Tel : 03-5734-2975 / Fax : 03-5734-3661

